ТИРОНЕТ – все о щитовидной железе Для специалистов Журнал Тиронет Архив журнала 2002 год № 4
Врожденный гипотиреоз
Thyroid international 3 – 2002
Дельберт А. Фишер (Delbert A. Fisher, M.D.), Сан Хуан Капистрано, Калифорния, США
Русский перевод к.м.н. Фадеева В.В. (примечания и комментарии переводчика отмечены*)
ЭТИОЛОГИЯ ВРОЖДЕННОГО ГИПОТИРЕОЗА
После внедрения скрининговых программ стали активно развиваться клинические исследования детей и молекулярная генетика ВГ, достижения которой принципиальным образом изменили наши представления об этиологии этого заболевания. Частота новых случаев ВГ составляет 1 на 3500 - 4000 новорожденных [27, 28]. Современные представления об этиологии ВГ кратко суммирует табл. 1. Примерно в 70% случаев речь идет о дисгенезии щитовидной железы: об эктопии или о гипогенезии-агенезии [24, 28, 30]. Сообщалось, что её распространенность может достигать 85% случаев ВГ [23]. Примерно у 2/3 детей с дисгенезией щитовидной железы выявляется резидуальная тиреоидная ткань [28, 29]. Дисгенезия чаще встречается у девочек (соотношение девочки/мальчики - 2/1), реже среди лиц африканского (1:32000) и чаще среди лиц испанского происхождения (1:2000) [27, 29, 31]. Примерно в 2% случаев ВГ речь идет о семейных формах заболевания, при которых описаны мутации в гомеобоксах генов TTF-1, TTF-2 и PAX-8 [30, 31]. У детей с ВГ повышена распространенность различных врожденных аномалий (7 - 20% против 3,2% в общей популяции); дефекты включают в себя врожденные пороки сердца, врожденный вывих бедра, расщелину неба, синдром Дауна, трисомию 18 и другие дисморфные синдромы (Beckwith, Sotos) [22, 32]. По сравнению с истинным ВГ, пороки развития чаще встречаются у детей с транзиторным ВГ, который может быть обусловлен поступлением в организм мегадоз йода с антисептиками, родовой асфиксией, респираторным дистресс синдромом или другими заболеваниями, ассоциированы с пороками развития неонатального периода [32]. При синдроме Дауна ВГ встречается в 1 из 41 случая, что превышает его популяционную распространенность в 100 раз [33]. При семейных формах ВГ встречаются пороки развития, ассоциированные с известными генетическими мутациями. При значительно чаще встречающихся несемейных формах, причина сопутствующих пороков развития остается невыясненной.
Транзиторный врожденный гипотиреоз (низкий Т4 при повышенном ТТГ) описан как следствие введения в организм матери или ребенка мегадоз йода и его органических соединений, приема матерью тиреостатических препаратов и других медикаментов (амиодарон, противоастматические средства), а также вследствие циркуляции у матери антител, блокирующих рецептор ТТГ [22, 23, 34, 35]. Увеличение щитовидной железы у новорожденного может свидетельствовать о наличии у него транзиторного гипотиреоза, индуцированного медикаментами или зобогенами, однако у большей части детей с транзиторным гипотиреозом размер щитовидной железы не увеличен как по данным пальпации, так и УЗИ. Захват йода может быть подавлен как самим йодом, так и антителами к рецептору ТТГ. Продолжительность транзиторного гипотиреоза, индуцированного медикаментами, обычно составляет 1 - 2 недели, но может достигать 1 - 4 месяцев в случае его развития под воздействием блокирующих антител к рецептору ТТГ, период полужизни которых достигает 2 недель [35]. Лечение транзиторного гипотиреоза необходимо только в тяжелых случаях и при его сохранении на протяжении более 1 - 2 недель.
Транзиторная гипертиротропинемия, при которой определяется повышенный уровень ТТГ и нормальный Т4, является достаточно редким расстройством. Основными причинами транзиторного и лёгкого нарушения функции щитовидной железы является её дисгенезия, дисгормоногенез или блокирующие антитела к рецептору ТТГ [36]. [*В регионах йодного дефицита транзиторная гипертиротропинемия редким феноменом не является (Ф.В)].
Идиопатическая гипертиротропинемия редкое расстройство, описанное в Японии, где оно встречается с частотой 1 случай на 18000 новорожденных [37]. В недавней работе на протяжении 2 - 7 лет были отслежены 16 случаев идиопатической гипертиротропинемии; уровень ТТГ у новорожденных сохранялся повышенным до 17 - 77 мЕд/л в течение 2 - 7 недель, уровень Т4, Т3 и свободного Т4, а также основной обмен и захват радиоактивного йода были в норме. Ответ ТТГ в тесте с ТРГ был повышен, антитела к рецептору ТТГ не определялись. Уровень ТТГ спонтанно нормализовался у 11 из 16 детей в течение 6 месяцев, но усиленный ответ в тесте с ТРГ сохранялся на протяжении 3 - 7 лет. У всех пациентов определялось адекватное повышение уровня Т3 в ответ на введение ТТГ, исключающее дефекты гормоногенеза. Кроме того, в течение 5 - 7 лет у 3 из 16 пациентов сформировался небольшой диффузный зоб. Причина этого расстройства остается неизвестной.
Нарушения, приводящие к ВГ и связанные с тиреоидным дисгормоногенезом, суммированы в таблице 2. Функция щитовидной железы состоит в захвате и концентрировании йода из крови, синтезе и секреции тиреоидных гормонов. Основными субстратами для синтеза тиреоидных гормонов являются йод и тирозин. Процесс синтеза тиреоидных гормонов стимулируется при связывании ТТГ с рецепторами фолликулярных клеток с последующей внутриклеточной трансдукцией сигнала G-белками и продукцией цАМФ (рис. 1). Процессы, стимулируемые цАМФ, включают: транспорт йодида через клеточную мембрану; синтез тиреоглобулина; окисление и органификацию йодида на мембране клеток, обращенной к коллоиду; активацию эндоцитоза коллоида и образование внутриклеточных фаголизосом, а также гидролиз тиреоглобулина (ТГ) и высвобождение монойодтирозинов и дийодтирозинов, Т4 и Т3. Йодтирозины активно дейодируются в тироцитах, Т4 и Т3 высвобождаются в кровь. Кроме того, преимущественно по лимфатической системе щитовидной железы, в циркуляцию попадают существенные количества ТГ.
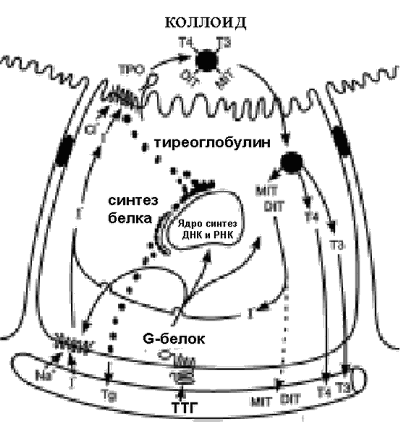
Рис. 1. Схема синтеза и секреции тиреоидных гормонов в фолликулярных клетках. ТPО - тиреоидная пероксидаза; MIT - монойодтирозин; DIT - дийодтирозин; Тg - тиреоглобулин. Натрий-йодидный симпортер (NIS) - мембранный белок, обеспечивающий транспорт йода внутрь клетки. Пендрин, осуществляющий симпор йода и хлора через апикальную мембрану, поставляет йод для органификации. ТТГ стимулирует транспорт йода и синтез тиреоглобулина. Секреция тиреоидных гормонов осуществляется после стимуляции тиротропином эндоцитоза коллоида и деградации фаголизосом. Высвобождающиеся наряду с тиреоидными гормонами МИТ и ДИТ активно дейодируются и йод вновь поступает в тироциты.
Большинство вариантов тиреоидного дисгормоногенеза наследуется аутосомно-рецессивно. За исключением большей семейной ассоциации и тенденции к развитию у пациентов зоба, клиническая манифестация ВГ, развившегося вследствие биохимических дефектов, аналогична таковой при дисгенезии щитовидной железы. Увеличение щитовидной железы может определяться уже при рождении, но, в большинстве случаев, развитие зоба отсрочено. В последние годы этой проблеме было посвящено несколько обзоров литературы [24, 38 - 41]. Молекулярно-генетические методы исследования, направленные на определение конкретных генетических дефектов у детей с ВГ в результате тиреоидного дисгормоногенеза, в настоящее время не поучили широкого распространения.
Табл. 1. Этиология врожденного гипотиреоза
| Тип нарушения | Доля (%) от всех случаев | Причины |
| А. Дисгенезия щитовидной железы Эктопия Агенезия или гипогенезия | 45% 25% | <3% мутации TTF-1, TTF-2, PAX-8 Возможно другие мутации? |
| В. Дисгормоногенез Нечувствительность к ТТГ Дефекты транспорта йода Дефекты органификации Дефекты тиреоглобулина Дефекты йодтирозин-дейодиназы | 20% | см. табл. 2 |
| С. Транзиторный гипотиреоз | 4%* | Материнские антитела блокирующие рецепторы ТТГ Тиростатики Амиодарон Высокие дозы йода Другие факторы |
| D. Транзиторная идиопатическая гипртиротропинемия | <1%* | Факторы, перечисленные выше (С), действующие менее интенсивно Дисгенезия щитовидной железы при достаточно большом объеме резидуальной ткани Легкий дисгормоногенез Идиопатическая |
| Е. Гипоталамо-гипофизарные нарушения Гипоталамо-гипофизарные дисгенезии Функциональный гипопитуитаризм Дефицит ТТГ | 5% | Мутации генов SHH, SIX-3, ZIC-2, HESX-1, Pit-1, Prop-1 Мутации гена b-ТТГ |
* Распространенность транзиторного ВГ и гипертиротропинемии в Европе и других регионах йодного дефицита достигает 20 - 25% случаев [26]
Табл. 2. Врожденные дефекты, обуславливающие дефицит продукции или эффектов тиреоидных гормонов
[Cмотреть таблицу]
Вторичный (гипоталамо-гипофизарный) гипотиреоз - еще один вариант ВГ, заболеваемость которым составляет 1 случай на 20000 - 50000 новорождённых. Вторичный ВГ не выявляется при скрининге, основанном на определении одного только ТТГ [23]. Вторичный ВГ встречается при таких расстройствах, как анэнцефалия, голопрозэнцефалия, септо-оптическая дисплазия, гипоплазии и аплазии гипофиза, парциальном или тотальном гипопитуитаризме. Патогенез большинства этих расстройств остается неизвестным, однако у детей с голопрозэнцефалией были описаны мутации трех генов: SHH, SIX-3 и ZIC-2 [42 - 44]. Мутация гена HESX-1 ассоциирована с септо-оптической дисплазией, включающей пороки развития среднего мозга и гипоплазию гипофиза [45]. У грызунов развитие гипоталамуса обуславливают гены SF-1, LHX-1 и LHX-4 [46]. Гены Prop-1 и Pit-1 являются терминальными факторами в каскаде генов программирующих развитие и функционирование клеток гипофиза, продуцирующих гормон роста, пролактин и b-субъедницу ТТГ. Мутации генов Prop-1 и Pit-1 описаны у пациентов с семейным гипопитуитаризмом [47]. Мутации гена b-субъединицы ТТГ также были писаны как редкая причина дефицита ТТГ [48].




